Swissmedic ist für die Überwachung der Sicherheit der Arzneimittel zuständig. Dies umfasst die Entgegennahme und Evaluation von Meldungen zu Nebenwirkungen von Medikamenten und Impfstoffen einschliesslich Covid-Impfstoffen. Swissmedic beantwortet jedoch keine Anfragen zu individuellen Therapie- oder Impffragen und gibt keine entsprechenden Empfehlungen ab. Bitte wenden Sie sich hierfür an Ihren Arzt oder Ihre Ärztin.
Das Schweizer Heilmittelgesetz sieht vor, dass Konsumentinnen und Konsumenten, Patientinnen und Patienten und deren Organisationen sowie interessierte Dritte der Swissmedic unerwünschte Wirkungen von Heilmitteln und Vorkommnisse melden können.
Bitte denken Sie daran, dass diese Meldung nicht ein Gespräch mit Ihrer Ärztin/Ihrem Arzt oder Apothekerin/Apotheker ersetzt, wenn Sie aufgrund unerwünschter vermuteter Nebenwirkungen oder eines Vorkommnisses besorgt sind.
Eine allgemeine Nebenwirkung eines Arzneimittels oder eine vermutete Nebenwirkung in Zusammenhang mit einem Covid-19-Impfstoff melden
Privatpersonen können alle Meldungen über vermutete Nebenwirkungen von Humanarzneimitteln über ein Web-Formular bei Swissmedic einreichen. Sie können eine Nebenwirkung für sich oder auch im Namen einer anderen Person wie etwa im Namen eines Kindes oder eines/einer Angehörigen melden.
Wichtige Hinweise zur Meldung durch Privatpersonen
Beachten Sie, dass eine Nebenwirkungsmeldung weder eine ärztliche Untersuchung noch eine Diagnose ersetzt. Auch wenn im Einzelfall ein zeitlicher Zusammenhang zwischen der Verabreichung eines Arzneimittels oder einer Impfung und dem Auftreten eines Symptoms oder einer Erkrankung besteht, bedeutet dies nicht zwingend, dass das Arzneimittel bzw. der Impfstoff auch tatsächlich die Ursache war. Andere mögliche Ursachen, die allenfalls gezielte therapeutische Massnahmen erforderlich machen, können nur mit ärztlicher Diagnose ausgeschlossen werden.
Wenn Sie Symptome bemerken, die eine Nebenwirkung sein könnten, wenden Sie sich in erster Linie an diejenige Stelle, welche Ihnen die Medikamente verschrieben, abgegeben oder verabreicht hat. Konsultieren Sie bei Beschwerden immer ihre behandelnde Ärztin/ihren behandelnden Arzt. Medizinische Fachpersonen können beurteilen, ob es sich um eine meldepflichtige Nebenwirkung oder eher um Beschwerden anderer Ursache handelt. Bitten Sie allenfalls ihre medizinische Fachperson (Ärztin/Arzt, Apothekerin/Apotheker), die Nebenwirkung zu melden.
Mit der Meldung von Nebenwirkungen oder entsprechenden Verdachtsfällen leisten Sie einen wichtigen Beitrag für sichere Arzneimittel und Impfstoffe. Bitte haben Sie aber Verständnis dafür, dass Swissmedic keine individuellen Therapie- oder Gesundheitsfragen beantwortet und keine entsprechenden Empfehlungen abgibt.
Allgemeine Informationen
FAQ
Notwendigkeit der Pharmacovigilance
Arzneimittel werden über mehrere Jahre entwickelt. Wirksamkeit und Sicherheit eines neuen Präparates werden in der Regel an wenigen tausend, nach streng definierten Kriterien selektionierten und engmaschig kontrollierten ProbandInnen und PatientInnen untersucht. Deshalb können während der klinischen Entwicklung nur sehr häufig auftretende, meist durch den pharmakologischen Mechanismus bedingte unerwünschte Wirkungen beobachtet werden.
Nach Markteinführung wird eine viel grössere, häufig auch polymorbide Population exponiert, was zu einer Änderung des bis anhin bekannten Sicherheitsprofils eines Arzneimittels führen kann. Unerwünschte Wirkungen können nun häufiger beobachtet werden und zwar auch solche, die nur sporadisch und unabhängig von den pharmakologischen Eigenschaften der Substanz auftreten. Diese unerwünschten, in der täglichen Praxis beobachteten Wirkungen einer Arzneimitteltherapie müssen rasch gemeldet werden. Durch konsequente Weiterleitung solcher Informationen an das nationale Pharmacovigilance Zentrum der Swissmedic können bisher unerkannte Risiken aufgedeckt und angegangen werden.
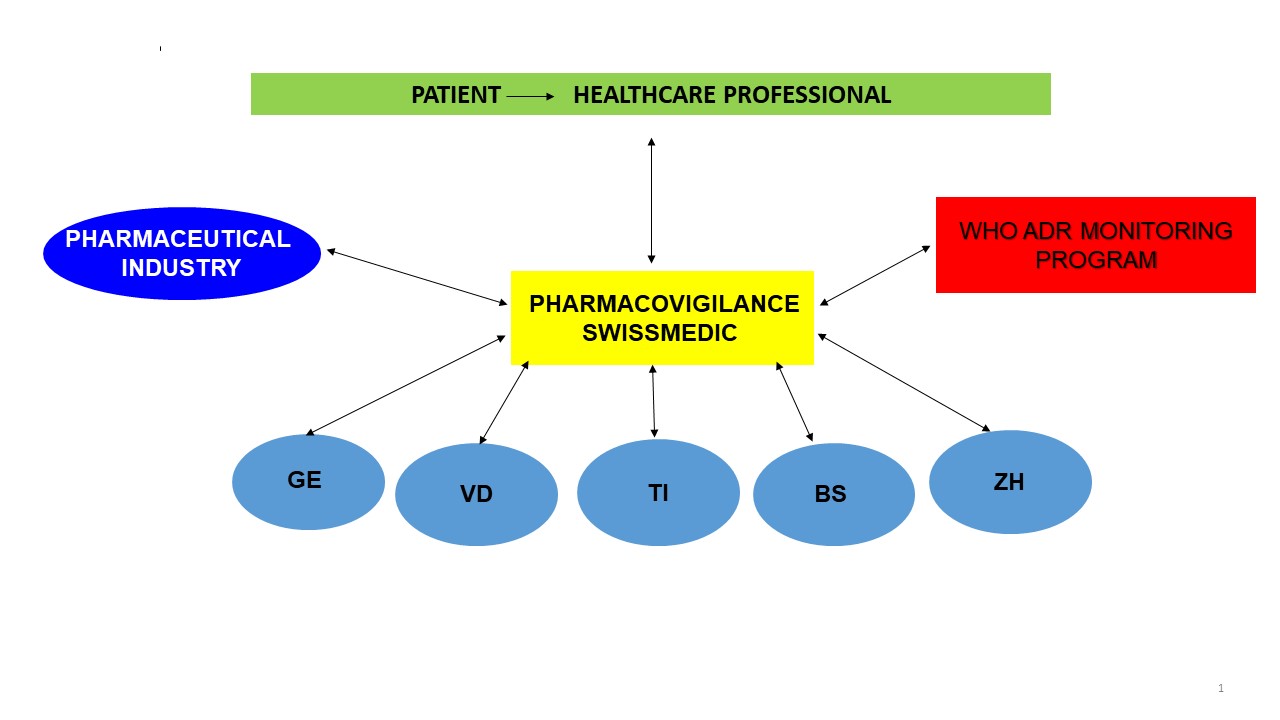
Das nationale Pharmacovigilance Zentrum der Swissmedic nimmt Meldungen von unerwünschten Arzneimittelwirkungen entgegen und bearbeitet sie. Dabei wird das nationale Pharmacovigilance Zentrum von fünf regionalen Zentren unterstützt, die einer universitären Abteilung für klinische Pharmakologie angegliedert sind und insbesondere Meldungen von medizinischen Fachpersonen mit hohem Signalwert bearbeiten. Die pharmazeutische Industrie leitet ihrerseits an Swissmedic Meldungen unerwünschter Wirkungen weiter, die bei ihr eingegangen sind. Das nationale Pharmacovigilance Zentrum arbeitet mit dem internationalen Zentrum für Arzneimittelsicherheit der Weltgesundheitsorganisation WHO eng zusammen.
Gemäss Heilmittelgesetz müssen unerwünschte Wirkungen gemeldet werden, die schwerwiegend oder unbekannt sind, oder in der Fachinformation des betreffenden Medikamentes ungenügend beschrieben werden.
Schwerwiegende unerwünschte Wirkungen sind solche, die
- tödlich verlaufen
- lebensbedrohend sind
- zu einer Hospitalisation oder deren Verlängerung führen
- schwere oder bleibende Schäden verursachen
- sonst als medizinisch wichtig zu beurteilen sind (z.B. wenn durch eine rechtzeitige medizinische Intervention eine der oben erwähnten Situationen hat vermieden werden können)
Solche unerwünschte Wirkungen sollen innert 15 Tagen nach Kenntnis gemeldet werden, nicht schwerwiegende unerwünschte Wirkungen innert 60 Tagen.
Der Kausalzusammenhang zwischen einem Ereignis und einem Medikament muss nicht nachgewiesen werden: der Verdacht alleine reicht, um zu melden.
Meldungen über Missbrauch, Abhängigkeit und Sucht entsprechen zwar nicht der WHO-Definition einer unerwünschten Wirkung, da diese sich auf Ereignisse bezieht, die unter dem üblichen Gebrauch in normalen Dosen nicht vorkommen. Solche Meldungen sind trotzdem wichtig für die Beurteilung der Sicherheit eines Medikamentes und sollten deswegen ebenfalls an die zuständigen Stellen weitergeleitet werden.
Das Heilmittelgesetz sieht eine Meldepflicht vor für alle Fachleute, die zur Abgabe, Anwendung oder Verschreibung von Arzneimitteln berechtigt sind. Es besteht ferner eine Meldepflicht für pharmazeutische Firmen, die Arzneimittel herstellen oder verwendungsfertige Arzneimittel vertreiben.
Es steht PatientInnen ebenfalls frei, unerwünschte Wirkungen einer Arzneimitteltherapie zu melden. Eine Rücksprache mit dem Hausarzt, der Hausärztin resp. eine gemeinsame Meldung haben den Vorteil, dass genaue Angaben zu relevanten Untersuchungsergebnissen gemacht werden können; sie ist jedoch nicht zwingend.
Privatpersonen
Patientinnen und Patienten, Angehörige oder interessierte Dritte können auch ohne medizinische Fachkenntnisse Nebenwirkungen und Vorkommnisse elektronisch an Swissmedic melden. Der Eingang der Meldung wird automatisch innerhalb der Anwendung bestätigt. Es werden keine zusätzlichen Eingangsbestätigungen per Mail verschickt.
Medizinische Fachpersonen/Angehörige von Gesundheitsberufen
Elektronische Meldungen über das ElViS-Portal sind der bevorzugte Weg für medizinische Fachpersonen. Mit ElViS können zusätzlich auch fallbezogene Dokumente wie z.B. Labor- oder Austrittsberichte übermittelt werden.
Firmen
Zulassunginhaberinnen können Verdachtsfälle unerwünschter Arzneimittelwirkungen entweder über das ElViS-Portal (Elektronisches Vigilance System) oder über ein Gateway zum elektronischen Austausch von Einzelfallmeldungen übermitteln.
Das Pharmacovigilance Team von Swissmedic überprüft die eingegangenen Meldungen sorgfältig nach neuen Risiken. Wenn es solche identifiziert, ermittelt es den Handlungsbedarf und leitet in Zusammenarbeit mit den für das Präparat zuständigen Abteilungen von Swissmedic die entsprechenden Massnahmen ein.
Support/Kontakt
Adresse
Swissmedic
Einheit Pharmacovigilance
Hallerstrasse 7
3012 Bern (Schweiz)
Hinweise zu Anfragen
Bitte haben Sie Verständnis, dass Swissmedic weder individuelle Therapie- oder Impffragen beantworten noch entsprechende Empfehlungen abgeben kann. Wenden Sie sich zur Diagnose und Therapie der Symptome oder Beschwerden immer an Ihre Ärztin oder Ihren Arzt.
Letzte Änderung 15.12.2025

