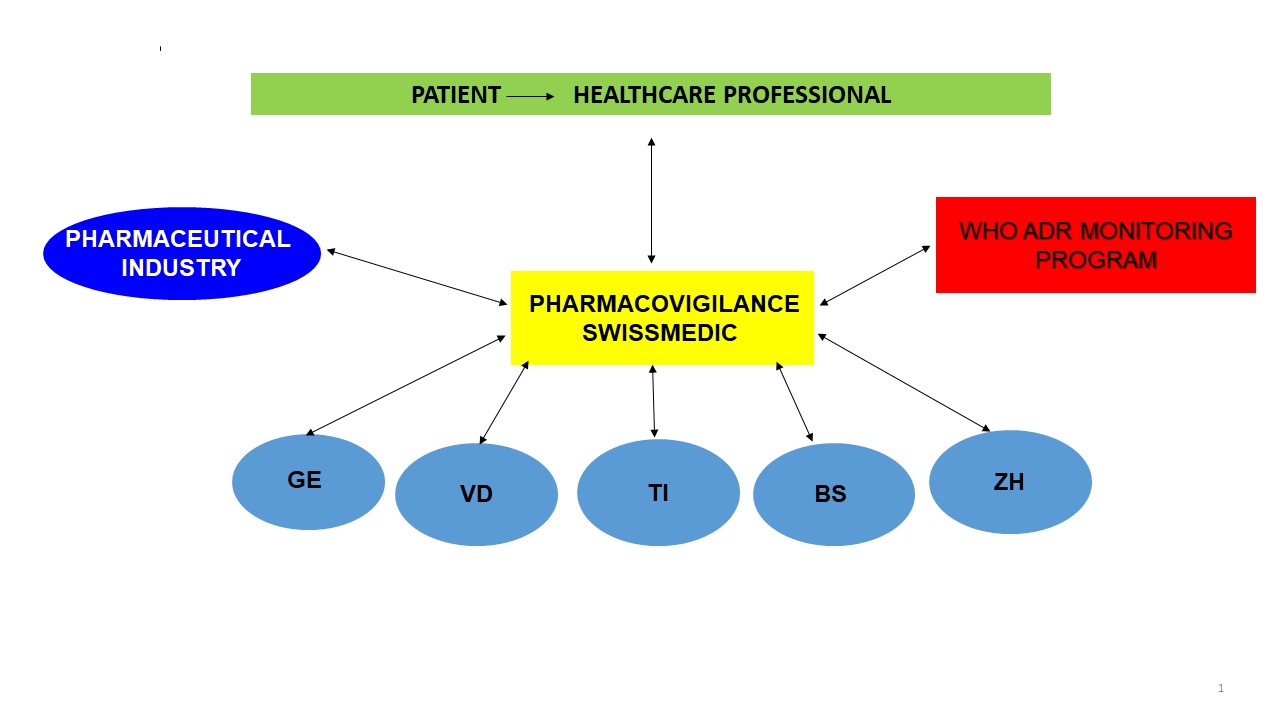
Ai sensi della legge sugli agenti terapeutici devono essere notificati gli effetti indesiderati gravi o non ancora conosciuti, ovvero quelli descritti in modo insufficiente nell’informazione professionale del medicamento in questione.
Reazioni avverse gravi sono quelle
- con decorso mortale;
- che rappresentano un pericolo di morte;
- che provocano una degenza in ospedale o la prolungano;
- che causano danni gravi o permanenti;
- che sono da considerare importanti dal punto di vista medico (quando, per esempio, un intervento medico tempestivo permette di evitare le situazioni sopraccitate).
Queste reazioni avverse devono essere segnalate entro 15 giorni da quando sono stati notati, le reazioni non gravi entro 60 giorni.
Il nesso causale tra una reazione e un medicamento non deve essere provato: il solo sospetto è sufficiente perché venga notificato.
Le notifiche di abuso, dipendenza e tossicomania non corrispondono strettamente alla definizione dell'OMS di una reazione avversa da farmaco, poiché si riferiscono a casi che non avvengono a posologia normale. Ciò nonostante queste notifiche sono importanti per la valutazione della sicurezza di un medicamento e per questo motivo devono pure essere trasmesse all'ente competente.