27.02.2019
Update: Correzione dei nuovi documenti normativi eCTD Swiss M1 Specification e Swiss eCTD Validation Criteria
A causa di piccoli errori presenti nell’eCTD M1 Specification e nel relativo eCTD Validation Criteria, i due documenti devono essere corretti. Per esigenze tecniche viene mantenuto il numero di versione 1.4.
Si coglie inoltre l’occasione per precisare alcuni punti ancora dubbi.
Nella versione 1.4 sono state apportate le seguenti correzioni:
- Nel documento eCTD Validation Criteria:
- il nome della Directory 151-infoaccordappIVguidelinebioequivalence non è corretto e deve essere sostituito con 151-infoaccordappivguidelinebioequivalence. IV non deve essere scritto a lettere maiuscole.

- Nel documento Swiss M1 Specification:
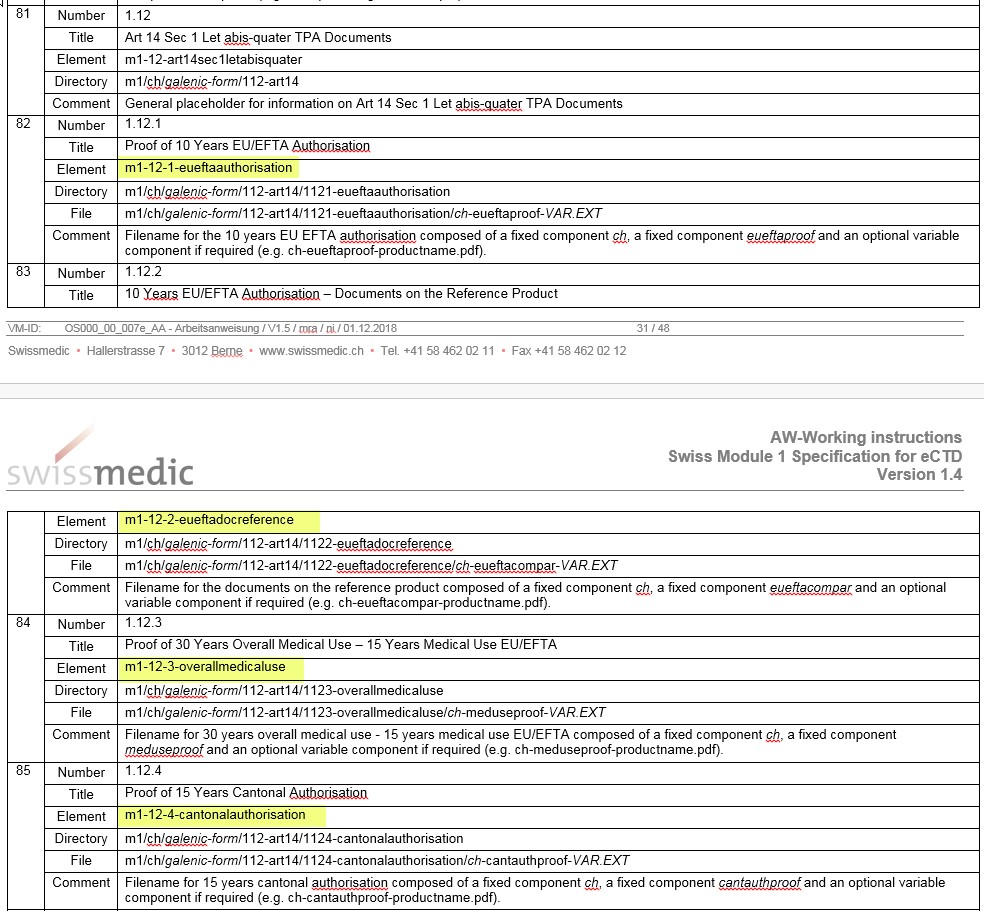
- I nuovi elementi riportati nella Section 1.12 nella Table 4 non sono scritti correttamente e vengono uniformati all’ortografia in base al DTD:
- 1.8.2 Risk Management System. Nella Table 1 mancava il trattino che è stato nuovamente aggiunto.

- Nella Table 4, il trattino in 1.2.1 è diverso da quello in 1.2.2. La grafia del trattino è stata uniformata.

Le seguenti correzioni sono state annotate e saranno apportate successivamente nella versione 1.5. Una tempistica concreta circa la pubblicazione della versione 1.5 sarà comunicata in futuro.
- Nel documento Swiss M1 Specification:
- Nella Table 1 non è necessario indicare nulla nelle colonne «Fixed Component of Filename» e «Life Cycle Operator» in corrispondenza con la riga 1.2.2.

- Gli application types pi e eas non sono più necessari ai sensi dell’OATer IV e vengono cancellati dalla tabella.
- Nel documento eCTD Validation Criteria:
- Immissione errata in File-Folder Structure & Names. Vi sono differenze fra M1 Specification e Validation Criteria. Il Fixed component di 1.2.2.20 deve essere foart13.

Alle domande rivolte a Swissmedic rispondiamo nel seguente modo:
Come si deve svolgere un Life Cycle in relazione alle Sections cancellate (p.es. 1.2.2.4, 1.2.2.5, ecc.)? Nella M1 Specification, le Sections cancellate sono contrassegnate dalla dicitura «this section is no longer applicable...».
Le seguenti grafie nel documento Swiss M1 Spec, Table 1 e Table 4 sono effettivamente corrette?
Risposta:
- Operazione replace/delete in un documento esistente in una Section cancellata -> Se qui si svolgesse un Life Cycle, scatterebbe la regola 15.BP3 e si attiverebbe un avviso. La Sequence continua a essere valida.
- Operazione new in una Section cancellata -> qui non si dovrà più svolgere un Life Cycle. La regola 15.BP3 attiva un avviso.
- In generale si può affermare che i documenti che finora erano inseriti in Sections cancellate in questo modo non sono più attuali o vengono sostituiti da nuovi moduli in un’altra Section.
- Life Cycle in un documento esistente nella Section 1.5.3 appena cancellata -> Qui non è più previsto un Life Cycle.
Risposta:
- 1.2.2.16 Form PSUR/PBRER for Human Medicines = l’assenza di spazi vuoti è intenzionale
- 1.2.2.23 Form Application for Recognition of Orphan Drug Status = la parola Recognition è scritta intenzionalmente con l’iniziale maiuscola
- 1.7.4 FDA Decision = il singolare è intenzionale
- 1.4.1 Quality (Leaf) = la mancata specificazione di Expert è intenzionale
- 1.4.2 Nonclinical (Leaf) = la mancata specificazione di Expert è intenzionale
- 1.4.3 Clinical (Leaf) = la mancata specificazione di Expert è intenzionale

