27.02.2019
Update: Korrektur der neuen eCTD-Vorgabedokumente Swiss M1 Specification und Swiss eCTD Validation Criteria
Aufgrund kleiner Fehler in der eCTD M1 Specification und der dazugehörigen eCTD Validation Criteria müssen die beiden Dokumente korrigiert werden. Aufgrund technischer Notwendigkeiten wird hierbei die Versionsnummer 1.4 beibehalten.
Zusätzlich sollen an dieser Stelle noch Unklarheiten genauer erklärt werden.
Folgende Korrekturen wurden in der Version 1.4 vorgenommen:
- In Dokument eCTD Validation Criteria:
- Ordnername 151-infoaccordappIVguidelinebioequivalence ist nicht korrekt und muss 151-infoaccordappivguidelinebioequivalence heissen. Die Grossschreibung von IV war falsch.

- In Dokument Swiss M1 Specification:
- Schreibweise der neuen Elemente in Section 1.12 in Table 4 ist falsch und wird an die korrekte Schreibweise in der DTD angeglichen:
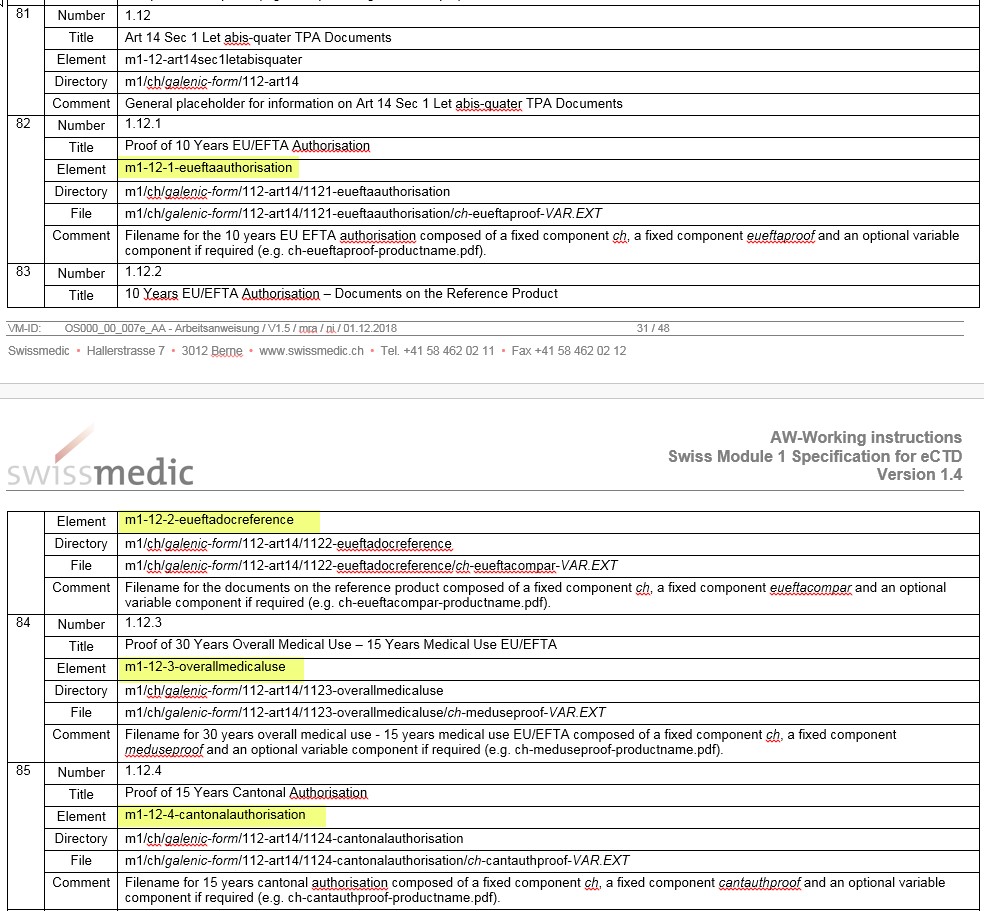
- 1.8.2 Risk-Management System. Der Bindestrich hat in Table 1 gefehlt, wurde wieder eingefügt

- Bindestrich in 1.2.1 unterscheidet sich von 1.2.2 in Table 4. Die Schreibweise des Bindestrichs wurde angeglichen

Folgende Korrekturen sind vorgemerkt für eine zukünftige Version 1.5 und werden dort später korrigiert. Eine konkrete zeitliche Planung zur Veröffentlichung der Version 1.5 wird noch kommuniziert.
- In Dokument Swiss M1 Specification:
- In der Table 1 ist bei 1.2.2 kein fixed component of filename und kein life cycle operator notwendig

- Application types pi und eas sind gemäss HMV4 nicht mehr notwendig und werden aus der Tabelle gelöscht.
- In Dokument eCTD Validation Criteria:
- Fehlerhafter Eintrag in File-Folder Structure & Names. Es gibt Unterschiede zwischen der M1 Specification und der Validation Criteria. Fixed component von 1.2.2.20 soll foart13 sein.

In Bezug auf an Swissmedic gerichtete Fragen nehmen wir wie folgt Stellung:
Antwort:
- Operation replace/delete auf ein bestehendes Dokument in einer gelöschten Section -> Sollte es hier einen Life Cycle geben, schlägt die Regel 15.BP3 an und gibt eine Warnung aus. Die Sequence ist weiterhin valid.
- Operation new auf eine gelöschte Section -> ein Life Cycle soll hier nicht mehr stattfinden. Die Regel 15.BP3 gibt eine Warnung aus.
- Generell lässt sich sagen, das Dokumente, die in solcherart gelöschte Sections bisher eingeordnet waren, entweder nicht mehr aktuell sind oder über neue Formulare in einer anderen Section ersetzt werden.
- Life Cycle auf ein bestehendes Dokument in der neu gelöschten Section 1.5.3 -> Ein Life Cycle ist hier gar nicht zu erwarten.
Antwort:
- 1.2.2.16 Form PSUR/PBRER for Human Medicines = Schreibweise ohne Leerschläge ist gewollt
- 1.2.2.23 Form Application for Recognition of Orphan Drug Status = Grossschreibung Recognition ist gewollt
- 1.7.4 FDA Decision = Einzahl ist gewollt
- 1.4.1 Quality (Leaf) = fehlende Angabe von Expert ist gewollt
- 1.4.2 Nonclinical (Leaf) = fehlende Angabe von Expert ist gewollt
- 1.4.3 Clinical (Leaf) = fehlende Angabe von Expert ist gewollt
Weiteres Vorgehen
Aktuell werden beide eCTD-Vorgabedokumente in der Version 1.4 korrigiert. Sie werden innerhalb der nächsten Tage veröffentlicht und auf unserer Website aufgeschaltet.
Sollten weitere Fehler bekannt werden, die weitere Anpassungen nach sich ziehen, wird das zeitnah an dieser Stelle kommuniziert.

